FÜR ÄRZTE
SEARCH
Einschränkungen des Harmony® Tests
Mit NIPT-Verfahren wie dem Harmony® Test werden numerische chromosomale Störungen (Trisomie 21, 18, 13, X/Y) nachgewiesen. Das Besondere an diesen Verfahren ist, dass sie nicht-invasiv durchgeführt werden. Es wird lediglich das Blut der Mutter untersucht.
Ein NIPT-Verfahren kann eine Ultraschall-Untersuchung im ersten Trimenon nicht ersetzen. Das Ersttrimester-Screening bzw. der Ultraschall gegen Ende des 1. Trimenons erkennt etwaige Störungen an den kindlichen Organen und ist weiterhin unbedingt zu empfehlen.
Mit den bislang zur Verfügung stehenden cffDNA-Tests können Chromosomen-Mosaike, partielle Trisomien oder Translokationen nur unzureichend erkannt werden.
Für eine ausreichend sichere Identifizierung einer Chromosomenstörung des Ungeborenen muss der Anteil an zellfreier fetaler (kindlicher) DNA (cffDNA) („Fetal Fraction“) im mütterlichen Blut mindestens 4 % betragen 1. Mit zunehmendem Alter der Schwangerschaft steigt der Anteil kindlicher DNA im Blut der Mutter an (siehe auch unten stehende Grafik). Dies ist der Grund dafür, dass der Harmony® Test erst ab der SSW 10+0 durchgeführt werden kann.
 Abbildung 1: Abhängigkeit der „Fetal Fraction“ von der Schwangerschaftswoche (SSW) (modifiziert nach 2)
Abbildung 1: Abhängigkeit der „Fetal Fraction“ von der Schwangerschaftswoche (SSW) (modifiziert nach 2)
Weiterhin gibt es einen Zusammenhang zwischen dem mütterlichen Gewicht und der „Fetal Fraction“: Je höher das mütterliche Gewicht, desto niedriger ist im Durchschnitt der Anteil an fetaler DNA im mütterlichen Blut. Somit kann ein erhöhtes mütterliches Gewicht zum Auftreten eines niedrigen Anteils an zellfreier fetaler cffDNA (<4%) führen.
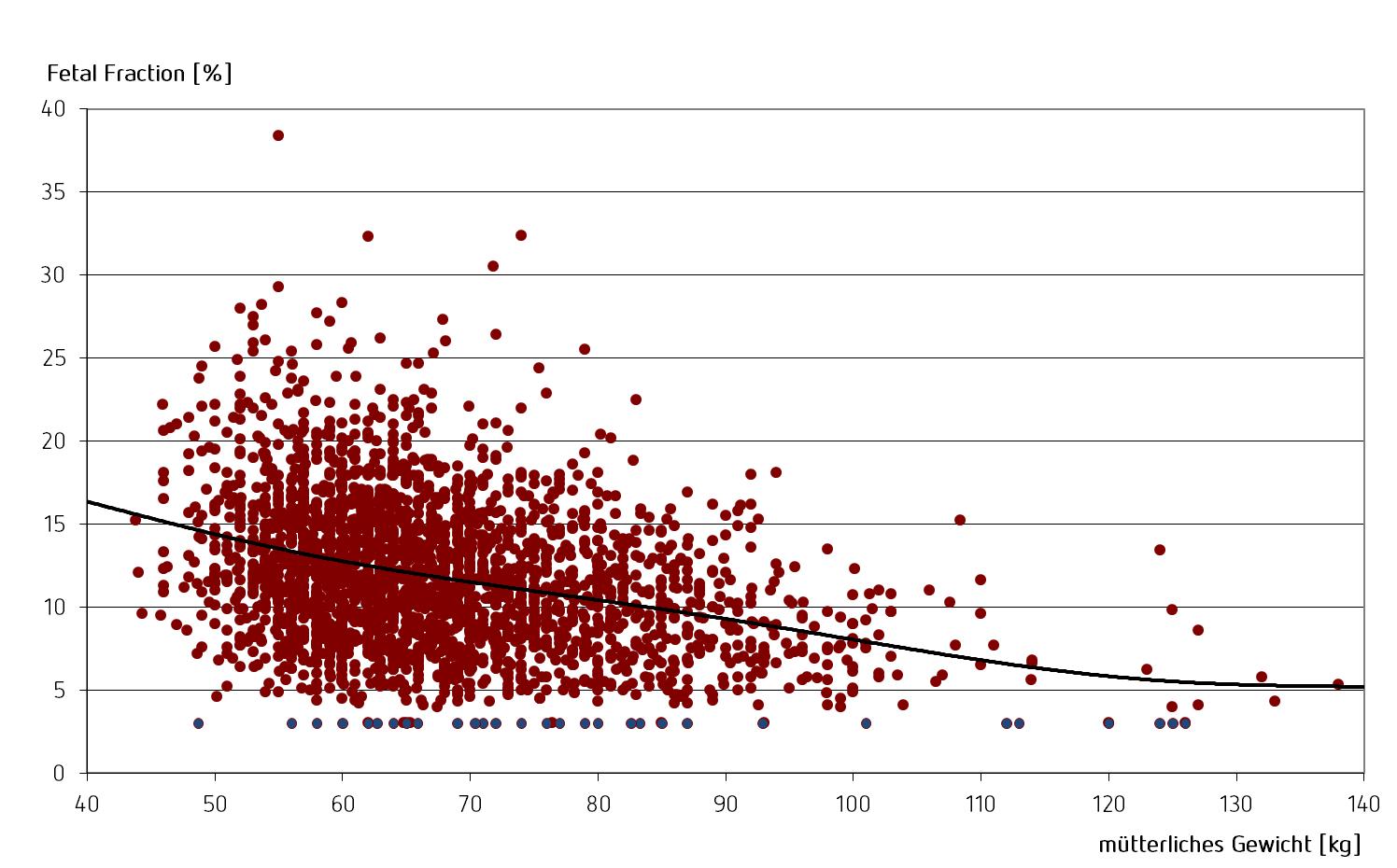 Abbildung 2: Abhängigkeit der „Fetal Fraction“ vom mütterlichen Gewicht (Daten Labor Enders, Stuttgart, Harmony® Test)
Abbildung 2: Abhängigkeit der „Fetal Fraction“ vom mütterlichen Gewicht (Daten Labor Enders, Stuttgart, Harmony® Test)Mit jedem Harmony® Test wird routinemäßig die „Fetal Fraction“ gemessen. Liegt die Fetal Fraction unter 4 %, ist der Test nicht auswertbar. Der Einsender wird darüber informiert, dass eine erneute Blutentnahme zu einem späteren Zeitpunkt zu empfehlen ist. Der Patientin entstehen durch einen nicht auswertbaren Harmony® Test keine Kosten.
Eine verschwiegene Eizellspende führt dazu, dass der Harmony® Test nicht auswertbar sein wird. Daher muss die Information einer erfolgten Eizellspende unbedingt auf dem Anforderungsschein mitgeteilt werden.
Ist diese Information angegeben, kann der Harmony® Test auch nach einer In-vitro-Befruchtung (IVF) uneingeschränkt durchgeführt werden.
Im Falle eines Vanishing Twins empfehlen wir, den Harmony® Test frühestens nach der 15. Schwangerschaftswoche bzw. mindestens acht Wochen nach dem Absterben des zweiten Feten durchzuführen7. Hintergrund ist, dass die Plazenta des abgestorbenen Zwillings häufig über mehrere Wochen persistiert und weiterhin zellfreie DNA freisetzt.
Der Harmony® Test ist nicht für den Einsatz bei Transplantationen, Krebserkrankung oder bei Aneuploidien der Mutter validiert. In diesen Fällen kann der Harmony® Test nicht durchgeführt werden.
Der Harmony® Test ist bei Zwillingsschwangerschaften anwendbar.
Eine aktuelle Studie zu Zwillingsanalysen von Judah et al. 2021 hat ergeben, dass sowohl Erkennungs- als auch Falsch-Positiv-Raten für die Trisomie 21 vergleichbar mit denen von Einlingsschwangerschaften sind3. Die Publikation verdeutlicht, dass die Leistungsfähigkeit des cfDNA-basierten Screenings bei Gemini-Schwangerschaften für die drei relevanten Trisomien durchweg besser ist als beim Ersttrimester-Screening.
Die Metaanalyse von Judah et al. basierte auf eigenen Studien der Nicolaides-Gruppe mit dem Harmony® Test sowie auf Publikationen mit MPSS*-Verfahren. Die Erkennungs- und Falsch-Positiv-Raten für NIPT bei Gemini-Schwangerschaften sind3:
| Trisomie | Erkennungsrate | Falsch-Positiv-Rate | Anzahl Trisomie-Fälle | Anzahl euploide Gemini-Schwangerschaften |
| 21 | ||||
| 18 | ||||
| 13 |
Eine Aussage über geschlechtschromosomale Störungen (X/Y-Analyse) wie z. B. Turner- oder Klinefelter-Syndrom ist bei Zwillingen derzeit nicht möglich.
Die unten stehende Tabelle gibt eine Übersicht, welche Variante des Harmony® Tests derzeit bei welcher Schwangerschaft möglich ist.
| Einling | Zwillinge | Mehr als zwei Feten | |
| Harmony® Test für T21 | |||
| Harmony® Test für T21/T18/T13 | |||
| Harmony® Test für T21/18/13 + X/Y-Analyse | |||
| Geschlechtsbestimmung |
Die Geschlechtsbestimmung ist bei Einlings- und Zwillingsschwangerschaften möglich. Die Mitteilung des fetalen Geschlechts erfolgt aufgrund des Gendiagnostik-Gesetzes ab SSW 14+0 (p.m.).
Bei einem geringen Prozentsatz der Fälle kann kein Testergebnis erzielt werden 4 5. Dies liegt im Wesentlichen an der Unterschreitung der 4 %-Grenze der Fetal Fraction, kann aber auch andere biologische Gründe, wie beispielsweise ein chromosomales Mosaik der Plazenta haben.
Ist der Gehalt an fetaler DNA im mütterlichen Blut zu gering, empfehlen wir für eine erneute Durchführung eine Blutabnahme zu einem späteren Zeitpunkt (nach etwa 2 Wochen). Unserer Erfahrung nach, können dann 50 % der Zweiteinsendungen erfolgreich ausgewertet werden. In den nicht auswertbaren Fällen muss gemeinsam mit der Patientin entschieden werden, ob z. B. ein erweitertes Ersttrimester-Screening oder evtl. doch eine invasive Diagnostik durchgeführt werden soll.
Trotz erheblicher Verbesserungen gegenüber den bisherigen nicht-invasiven Tests beträgt auch die Erkennungsrate des Harmony® Tests nicht 100%. Auch falsch-positive Ergebnisse können auftreten. Daher ist der Test als Screening-Test und nicht als diagnostischer Test anzusehen. Ein positives (auffälliges) Ergebnis sollte daher immer mit einer zweiten, diagnostischen, invasiven Methode (Chorionzottenbiopsie oder Amniozentese) mit anschließender Chromosomenanalyse bestätigt werden sofern aus dem Ergebnis eine Konsequenz abgeleitet werden soll.
Auch falsch-negative Ergebnisse können vorkommen. Dies ist insbesondere für die Trisomie 13 der Fall.
Der Harmony® Test erkennt nach derzeitigen Studien etwa 30 von 32 Trisomie 13 Fälle. Dies gilt auch für andere Nicht invasive pränatale Testverfahren. Eine Zusammenfassung aller bisherigen Studien zur Trisomie 13 ergab eine durchschnittliche Erkennungsrate von 93,8%6. Die Trisomie 13 wird jedoch in der qualifizierten Ultraschalluntersuchung im Rahmen des Ersttrimester-Screenings relativ gut erkannt.
- Ashoor G, Poon L, Syngelaki A, Mosimann B, Nicolaides KH. Fetal Fraction in Maternal Plasma Cell-Free DNA at 11–13 Weeks’ Gestation: Effect of Maternal and Fetal Factors. Fetal Diagn Ther 2012;31:237-243. ↩
- Wang E, Batey A, Struble C, Musci T, Song K, Oliphant A. Gestational age and maternal weight effects on fetal cell-free DNA in maternal plasma. Prenat Diagn. 2013 Jul;33(7):662-6. doi: 10.1002/pd.4119. Epub 2013 May 9. ↩
- Judah H. et al.: Cell-free DNA testing of maternal blood in screening for trisomies in twin pregnancy: updated cohort study at 10–14 weeks and metaanalysis. Ultrasound Obstet Gynecol 2021; 58: 178–189 ↩
- Lüthgens K, Grati FR, Sinzel M, Häbig K, Kagan KO. Confirmation rate of cell free DNA screening for sex chromosomal abnormalities according to the method of confirmatory testing. Prenat Diagn. 2020 Aug 17. doi: 10.1002/pd.5814. Epub ahead of print. PMID: 32804406. ↩
- Kagan, K. O., Sroka, F., Sonek, J., Abele, H., Lüthgens, K., Schmid, M., Wagner, P., Brucker, S., Wallwiener, D. and Hoopmann, M. (), First trimester screening based on ultrasound and cfDNA vs. first-trimester combined screening – a randomized controlled study. Ultrasound Obstet Gynecol. Accepted Author Manuscript. doi:10.1002/uog.18905 ↩
- Stokowski R, Wang E, White K, Batey A, Jacobsson B, Brar H, Balanarasimha M, Hollemon D, Sparks A, Nicolaides K, Musci TJ.: Clinical performance of non-invasive prenatal testing (NIPT) using targeted cell-free DNA analysis in maternal plasma with microarrays or next generation sequencing (NGS) is consistent across multiple controlled clinical studies. Prenat Diagn. 2015 Sep 1 ↩
- van Eekhout JCA, Bax CJ, Schuurman LVP, Becking EC, van der Ven AJEM, Van Opstal D, Boon EMJ, Macville MVE, Bekker MN, Galjaard RJH; Dutch NIPT Consortium. Performance of non-invasive prenatal testing in vanishing-twin and multiple pregnancies: results of TRIDENT-2 study. Ultrasound Obstet Gynecol. 2025 Sep 6. doi: 10.1002/uog.70015. Epub ahead of print. PMID: 40913805.
FÜR ÄRZTE
SEARCH
Einschränkungen des Harmony® Tests
Mit NIPT-Verfahren wie dem Harmony® Test werden numerische chromosomale Störungen (Trisomie 21, 18, 13, X/Y) nachgewiesen. Das Besondere an diesen Verfahren ist, dass sie nicht-invasiv durchgeführt werden. Es wird lediglich das Blut der Mutter untersucht.
Ein NIPT-Verfahren kann eine Ultraschall-Untersuchung im ersten Trimenon nicht ersetzen. Das Ersttrimester-Screening bzw. der Ultraschall gegen Ende des 1. Trimenons erkennt etwaige Störungen an den kindlichen Organen und ist weiterhin unbedingt zu empfehlen.
Mit den bislang zur Verfügung stehenden cffDNA-Tests können Chromosomen-Mosaike, partielle Trisomien oder Translokationen nur unzureichend erkannt werden.
Für eine ausreichend sichere Identifizierung einer Chromosomenstörung des Ungeborenen muss der Anteil an zellfreier fetaler (kindlicher) DNA (cffDNA) („Fetal Fraction“) im mütterlichen Blut mindestens 4 % betragen 1. Mit zunehmendem Alter der Schwangerschaft steigt der Anteil kindlicher DNA im Blut der Mutter an (siehe auch unten stehende Grafik). Dies ist der Grund dafür, dass der Harmony® Test erst ab der SSW 10+0 durchgeführt werden kann.
 Abbildung 1: Abhängigkeit der „Fetal Fraction“ von der Schwangerschaftswoche (SSW) (modifiziert nach 2)
Abbildung 1: Abhängigkeit der „Fetal Fraction“ von der Schwangerschaftswoche (SSW) (modifiziert nach 2)
Weiterhin gibt es einen Zusammenhang zwischen dem mütterlichen Gewicht und der „Fetal Fraction“: Je höher das mütterliche Gewicht, desto niedriger ist im Durchschnitt der Anteil an fetaler DNA im mütterlichen Blut. Somit kann ein erhöhtes mütterliches Gewicht zum Auftreten eines niedrigen Anteils an zellfreier fetaler cffDNA (<4%) führen.
 Abbildung 2: Abhängigkeit der „Fetal Fraction“ vom mütterlichen Gewicht (Daten Labor Enders, Stuttgart, Harmony® Test)
Abbildung 2: Abhängigkeit der „Fetal Fraction“ vom mütterlichen Gewicht (Daten Labor Enders, Stuttgart, Harmony® Test)Mit jedem Harmony® Test wird routinemäßig die „Fetal Fraction“ gemessen. Liegt die Fetal Fraction unter 4 %, ist der Test nicht auswertbar. Der Einsender wird darüber informiert, dass eine erneute Blutentnahme zu einem späteren Zeitpunkt zu empfehlen ist. Der Patientin entstehen durch einen nicht auswertbaren Harmony® Test keine Kosten.
Eine verschwiegene Eizellspende führt dazu, dass der Harmony® Test nicht auswertbar sein wird. Daher muss die Information einer erfolgten Eizellspende unbedingt auf dem Anforderungsschein mitgeteilt werden.
Ist diese Information angegeben, kann der Harmony® Test auch nach einer In-vitro-Befruchtung (IVF) uneingeschränkt durchgeführt werden.
Im Falle eines Vanishing Twins empfehlen wir, den Harmony® Test frühestens nach der 15. Schwangerschaftswoche bzw. mindestens acht Wochen nach dem Absterben des zweiten Feten durchzuführen7. Hintergrund ist, dass die Plazenta des abgestorbenen Zwillings häufig über mehrere Wochen persistiert und weiterhin zellfreie DNA freisetzt.
Der Harmony® Test ist nicht für den Einsatz bei Transplantationen, Krebserkrankung oder bei Aneuploidien der Mutter validiert. In diesen Fällen kann der Harmony® Test nicht durchgeführt werden.
Der Harmony® Test ist bei Zwillingsschwangerschaften anwendbar.
Eine aktuelle Studie zu Zwillingsanalysen von Judah et al. 2021 hat ergeben, dass sowohl Erkennungs- als auch Falsch-Positiv-Raten für die Trisomie 21 vergleichbar mit denen von Einlingsschwangerschaften sind3. Die Publikation verdeutlicht, dass die Leistungsfähigkeit des cfDNA-basierten Screenings bei Gemini-Schwangerschaften für die drei relevanten Trisomien durchweg besser ist als beim Ersttrimester-Screening.
Die Metaanalyse von Judah et al. basierte auf eigenen Studien der Nicolaides-Gruppe mit dem Harmony® Test sowie auf Publikationen mit MPSS*-Verfahren. Die Erkennungs- und Falsch-Positiv-Raten für NIPT bei Gemini-Schwangerschaften sind3:
| Trisomie | Erkennungsrate | Falsch-Positiv-Rate | Anzahl Trisomie-Fälle | Anzahl euploide Gemini-Schwangerschaften |
| 21 | ||||
| 18 | ||||
| 13 |
Eine Aussage über geschlechtschromosomale Störungen (X/Y-Analyse) wie z. B. Turner- oder Klinefelter-Syndrom ist bei Zwillingen derzeit nicht möglich.
Die unten stehende Tabelle gibt eine Übersicht, welche Variante des Harmony® Tests derzeit bei welcher Schwangerschaft möglich ist.
| Einling | Zwillinge | Mehr als zwei Feten | |
| Harmony® Test für T21 | |||
| Harmony® Test für T21/T18/T13 | |||
| Harmony® Test für T21/18/13 + X/Y-Analyse | |||
| Geschlechtsbestimmung |
Die Geschlechtsbestimmung ist bei Einlings- und Zwillingsschwangerschaften möglich. Die Mitteilung des fetalen Geschlechts erfolgt aufgrund des Gendiagnostik-Gesetzes ab SSW 14+0 (p.m.).
Bei einem geringen Prozentsatz der Fälle kann kein Testergebnis erzielt werden 4 5. Dies liegt im Wesentlichen an der Unterschreitung der 4 %-Grenze der Fetal Fraction, kann aber auch andere biologische Gründe, wie beispielsweise ein chromosomales Mosaik der Plazenta haben.
Ist der Gehalt an fetaler DNA im mütterlichen Blut zu gering, empfehlen wir für eine erneute Durchführung eine Blutabnahme zu einem späteren Zeitpunkt (nach etwa 2 Wochen). Unserer Erfahrung nach, können dann 50 % der Zweiteinsendungen erfolgreich ausgewertet werden. In den nicht auswertbaren Fällen muss gemeinsam mit der Patientin entschieden werden, ob z. B. ein erweitertes Ersttrimester-Screening oder evtl. doch eine invasive Diagnostik durchgeführt werden soll.
Trotz erheblicher Verbesserungen gegenüber den bisherigen nicht-invasiven Tests beträgt auch die Erkennungsrate des Harmony® Tests nicht 100%. Auch falsch-positive Ergebnisse können auftreten. Daher ist der Test als Screening-Test und nicht als diagnostischer Test anzusehen. Ein positives (auffälliges) Ergebnis sollte daher immer mit einer zweiten, diagnostischen, invasiven Methode (Chorionzottenbiopsie oder Amniozentese) mit anschließender Chromosomenanalyse bestätigt werden sofern aus dem Ergebnis eine Konsequenz abgeleitet werden soll.
Auch falsch-negative Ergebnisse können vorkommen. Dies ist insbesondere für die Trisomie 13 der Fall.
Der Harmony® Test erkennt nach derzeitigen Studien etwa 30 von 32 Trisomie 13 Fälle. Dies gilt auch für andere Nicht invasive pränatale Testverfahren. Eine Zusammenfassung aller bisherigen Studien zur Trisomie 13 ergab eine durchschnittliche Erkennungsrate von 93,8%6. Die Trisomie 13 wird jedoch in der qualifizierten Ultraschalluntersuchung im Rahmen des Ersttrimester-Screenings relativ gut erkannt.
- Ashoor G, Poon L, Syngelaki A, Mosimann B, Nicolaides KH. Fetal Fraction in Maternal Plasma Cell-Free DNA at 11–13 Weeks’ Gestation: Effect of Maternal and Fetal Factors. Fetal Diagn Ther 2012;31:237-243. ↩
- Wang E, Batey A, Struble C, Musci T, Song K, Oliphant A. Gestational age and maternal weight effects on fetal cell-free DNA in maternal plasma. Prenat Diagn. 2013 Jul;33(7):662-6. doi: 10.1002/pd.4119. Epub 2013 May 9. ↩
- Judah H. et al.: Cell-free DNA testing of maternal blood in screening for trisomies in twin pregnancy: updated cohort study at 10–14 weeks and metaanalysis. Ultrasound Obstet Gynecol 2021; 58: 178–189 ↩
- Lüthgens K, Grati FR, Sinzel M, Häbig K, Kagan KO. Confirmation rate of cell free DNA screening for sex chromosomal abnormalities according to the method of confirmatory testing. Prenat Diagn. 2020 Aug 17. doi: 10.1002/pd.5814. Epub ahead of print. PMID: 32804406. ↩
- Kagan, K. O., Sroka, F., Sonek, J., Abele, H., Lüthgens, K., Schmid, M., Wagner, P., Brucker, S., Wallwiener, D. and Hoopmann, M. (), First trimester screening based on ultrasound and cfDNA vs. first-trimester combined screening – a randomized controlled study. Ultrasound Obstet Gynecol. Accepted Author Manuscript. doi:10.1002/uog.18905 ↩
- Stokowski R, Wang E, White K, Batey A, Jacobsson B, Brar H, Balanarasimha M, Hollemon D, Sparks A, Nicolaides K, Musci TJ.: Clinical performance of non-invasive prenatal testing (NIPT) using targeted cell-free DNA analysis in maternal plasma with microarrays or next generation sequencing (NGS) is consistent across multiple controlled clinical studies. Prenat Diagn. 2015 Sep 1 ↩
- van Eekhout JCA, Bax CJ, Schuurman LVP, Becking EC, van der Ven AJEM, Van Opstal D, Boon EMJ, Macville MVE, Bekker MN, Galjaard RJH; Dutch NIPT Consortium. Performance of non-invasive prenatal testing in vanishing-twin and multiple pregnancies: results of TRIDENT-2 study. Ultrasound Obstet Gynecol. 2025 Sep 6. doi: 10.1002/uog.70015. Epub ahead of print. PMID: 40913805.
Einschränkungen des Harmony® Tests
Mit NIPT-Verfahren wie dem Harmony® Test werden numerische chromosomale Störungen (Trisomie 21, 18, 13, X/Y) nachgewiesen. Das Besondere an diesen Verfahren ist, dass sie nicht-invasiv durchgeführt werden. Es wird lediglich das Blut der Mutter untersucht.
Ein NIPT-Verfahren kann eine Ultraschall-Untersuchung im ersten Trimenon nicht ersetzen. Das Ersttrimester-Screening bzw. der Ultraschall gegen Ende des 1. Trimenons erkennt etwaige Störungen an den kindlichen Organen und ist weiterhin unbedingt zu empfehlen.
Mit den bislang zur Verfügung stehenden cffDNA-Tests können Chromosomen-Mosaike, partielle Trisomien oder Translokationen nur unzureichend erkannt werden.
Für eine ausreichend sichere Identifizierung einer Chromosomenstörung des Ungeborenen muss der Anteil an zellfreier fetaler (kindlicher) DNA (cffDNA) („Fetal Fraction“) im mütterlichen Blut mindestens 4 % betragen 1. Mit zunehmendem Alter der Schwangerschaft steigt der Anteil kindlicher DNA im Blut der Mutter an (siehe auch unten stehende Grafik). Dies ist der Grund dafür, dass der Harmony® Test erst ab der SSW 10+0 durchgeführt werden kann.
 Abbildung 1: Abhängigkeit der „Fetal Fraction“ von der Schwangerschaftswoche (SSW) (modifiziert nach 2)
Abbildung 1: Abhängigkeit der „Fetal Fraction“ von der Schwangerschaftswoche (SSW) (modifiziert nach 2)
Weiterhin gibt es einen Zusammenhang zwischen dem mütterlichen Gewicht und der „Fetal Fraction“: Je höher das mütterliche Gewicht, desto niedriger ist im Durchschnitt der Anteil an fetaler DNA im mütterlichen Blut. Somit kann ein erhöhtes mütterliches Gewicht zum Auftreten eines niedrigen Anteils an zellfreier fetaler cffDNA (<4%) führen.
 Abbildung 2: Abhängigkeit der „Fetal Fraction“ vom mütterlichen Gewicht (Daten Labor Enders, Stuttgart, Harmony® Test)
Abbildung 2: Abhängigkeit der „Fetal Fraction“ vom mütterlichen Gewicht (Daten Labor Enders, Stuttgart, Harmony® Test)Mit jedem Harmony® Test wird routinemäßig die „Fetal Fraction“ gemessen. Liegt die Fetal Fraction unter 4 %, ist der Test nicht auswertbar. Der Einsender wird darüber informiert, dass eine erneute Blutentnahme zu einem späteren Zeitpunkt zu empfehlen ist. Der Patientin entstehen durch einen nicht auswertbaren Harmony® Test keine Kosten.
Eine verschwiegene Eizellspende führt dazu, dass der Harmony® Test nicht auswertbar sein wird. Daher muss die Information einer erfolgten Eizellspende unbedingt auf dem Anforderungsschein mitgeteilt werden.
Ist diese Information angegeben, kann der Harmony® Test auch nach einer In-vitro-Befruchtung (IVF) uneingeschränkt durchgeführt werden.
Im Falle eines Vanishing Twins empfehlen wir, den Harmony® Test frühestens nach der 15. Schwangerschaftswoche bzw. mindestens acht Wochen nach dem Absterben des zweiten Feten durchzuführen7. Hintergrund ist, dass die Plazenta des abgestorbenen Zwillings häufig über mehrere Wochen persistiert und weiterhin zellfreie DNA freisetzt.
Der Harmony® Test ist nicht für den Einsatz bei Transplantationen, Krebserkrankung oder bei Aneuploidien der Mutter validiert. In diesen Fällen kann der Harmony® Test nicht durchgeführt werden.
Der Harmony® Test ist bei Zwillingsschwangerschaften anwendbar.
Eine aktuelle Studie zu Zwillingsanalysen von Judah et al. 2021 hat ergeben, dass sowohl Erkennungs- als auch Falsch-Positiv-Raten für die Trisomie 21 vergleichbar mit denen von Einlingsschwangerschaften sind3. Die Publikation verdeutlicht, dass die Leistungsfähigkeit des cfDNA-basierten Screenings bei Gemini-Schwangerschaften für die drei relevanten Trisomien durchweg besser ist als beim Ersttrimester-Screening.
Die Metaanalyse von Judah et al. basierte auf eigenen Studien der Nicolaides-Gruppe mit dem Harmony® Test sowie auf Publikationen mit MPSS*-Verfahren. Die Erkennungs- und Falsch-Positiv-Raten für NIPT bei Gemini-Schwangerschaften sind3:
| Trisomie | Erkennungsrate | Falsch-Positiv-Rate | Anzahl Trisomie-Fälle | Anzahl euploide Gemini-Schwangerschaften |
| 21 | ||||
| 18 | ||||
| 13 |
Eine Aussage über geschlechtschromosomale Störungen (X/Y-Analyse) wie z. B. Turner- oder Klinefelter-Syndrom ist bei Zwillingen derzeit nicht möglich.
Die unten stehende Tabelle gibt eine Übersicht, welche Variante des Harmony® Tests derzeit bei welcher Schwangerschaft möglich ist.
| Einling | Zwillinge | Mehr als zwei Feten | |
| Harmony® Test für T21 | |||
| Harmony® Test für T21/T18/T13 | |||
| Harmony® Test für T21/18/13 + X/Y-Analyse | |||
| Geschlechtsbestimmung |
Die Geschlechtsbestimmung ist bei Einlings- und Zwillingsschwangerschaften möglich. Die Mitteilung des fetalen Geschlechts erfolgt aufgrund des Gendiagnostik-Gesetzes ab SSW 14+0 (p.m.).
Bei einem geringen Prozentsatz der Fälle kann kein Testergebnis erzielt werden 4 5. Dies liegt im Wesentlichen an der Unterschreitung der 4 %-Grenze der Fetal Fraction, kann aber auch andere biologische Gründe, wie beispielsweise ein chromosomales Mosaik der Plazenta haben.
Ist der Gehalt an fetaler DNA im mütterlichen Blut zu gering, empfehlen wir für eine erneute Durchführung eine Blutabnahme zu einem späteren Zeitpunkt (nach etwa 2 Wochen). Unserer Erfahrung nach, können dann 50 % der Zweiteinsendungen erfolgreich ausgewertet werden. In den nicht auswertbaren Fällen muss gemeinsam mit der Patientin entschieden werden, ob z. B. ein erweitertes Ersttrimester-Screening oder evtl. doch eine invasive Diagnostik durchgeführt werden soll.
Trotz erheblicher Verbesserungen gegenüber den bisherigen nicht-invasiven Tests beträgt auch die Erkennungsrate des Harmony® Tests nicht 100%. Auch falsch-positive Ergebnisse können auftreten. Daher ist der Test als Screening-Test und nicht als diagnostischer Test anzusehen. Ein positives (auffälliges) Ergebnis sollte daher immer mit einer zweiten, diagnostischen, invasiven Methode (Chorionzottenbiopsie oder Amniozentese) mit anschließender Chromosomenanalyse bestätigt werden sofern aus dem Ergebnis eine Konsequenz abgeleitet werden soll.
Auch falsch-negative Ergebnisse können vorkommen. Dies ist insbesondere für die Trisomie 13 der Fall.
Der Harmony® Test erkennt nach derzeitigen Studien etwa 30 von 32 Trisomie 13 Fälle. Dies gilt auch für andere Nicht invasive pränatale Testverfahren. Eine Zusammenfassung aller bisherigen Studien zur Trisomie 13 ergab eine durchschnittliche Erkennungsrate von 93,8%6. Die Trisomie 13 wird jedoch in der qualifizierten Ultraschalluntersuchung im Rahmen des Ersttrimester-Screenings relativ gut erkannt.
- Ashoor G, Poon L, Syngelaki A, Mosimann B, Nicolaides KH. Fetal Fraction in Maternal Plasma Cell-Free DNA at 11–13 Weeks’ Gestation: Effect of Maternal and Fetal Factors. Fetal Diagn Ther 2012;31:237-243. ↩
- Wang E, Batey A, Struble C, Musci T, Song K, Oliphant A. Gestational age and maternal weight effects on fetal cell-free DNA in maternal plasma. Prenat Diagn. 2013 Jul;33(7):662-6. doi: 10.1002/pd.4119. Epub 2013 May 9. ↩
- Judah H. et al.: Cell-free DNA testing of maternal blood in screening for trisomies in twin pregnancy: updated cohort study at 10–14 weeks and metaanalysis. Ultrasound Obstet Gynecol 2021; 58: 178–189 ↩
- Lüthgens K, Grati FR, Sinzel M, Häbig K, Kagan KO. Confirmation rate of cell free DNA screening for sex chromosomal abnormalities according to the method of confirmatory testing. Prenat Diagn. 2020 Aug 17. doi: 10.1002/pd.5814. Epub ahead of print. PMID: 32804406. ↩
- Kagan, K. O., Sroka, F., Sonek, J., Abele, H., Lüthgens, K., Schmid, M., Wagner, P., Brucker, S., Wallwiener, D. and Hoopmann, M. (), First trimester screening based on ultrasound and cfDNA vs. first-trimester combined screening – a randomized controlled study. Ultrasound Obstet Gynecol. Accepted Author Manuscript. doi:10.1002/uog.18905 ↩
- Stokowski R, Wang E, White K, Batey A, Jacobsson B, Brar H, Balanarasimha M, Hollemon D, Sparks A, Nicolaides K, Musci TJ.: Clinical performance of non-invasive prenatal testing (NIPT) using targeted cell-free DNA analysis in maternal plasma with microarrays or next generation sequencing (NGS) is consistent across multiple controlled clinical studies. Prenat Diagn. 2015 Sep 1 ↩
- van Eekhout JCA, Bax CJ, Schuurman LVP, Becking EC, van der Ven AJEM, Van Opstal D, Boon EMJ, Macville MVE, Bekker MN, Galjaard RJH; Dutch NIPT Consortium. Performance of non-invasive prenatal testing in vanishing-twin and multiple pregnancies: results of TRIDENT-2 study. Ultrasound Obstet Gynecol. 2025 Sep 6. doi: 10.1002/uog.70015. Epub ahead of print. PMID: 40913805.

